- 1.1.1 熱力學(xué)學(xué)科的發(fā)展(P1)
- 2.1.2 熱力學(xué)課程(P2)
- 3.1.3 課程學(xué)習(xí)的方法和要求(P3)
- 4.2.1 流體的pvt關(guān)系概述(P4)
- 5.2.2 流體的狀態(tài)方程概述(P5)
- 6.2.3 維里型狀態(tài)方程(P6)
- 7.2.4 立方型狀態(tài)方程(van der Waals,RK)(P7)
- 8.2.5 其他立方型狀態(tài)方程(P8)
- 9.2.6 立方型狀態(tài)方程數(shù)值求解(P9)
- 10.2.7 立方型狀態(tài)方程迭代求解(P10)
- 11.2.8 多參數(shù)狀態(tài)方程(P11)
- 12.2.9 對應(yīng)狀態(tài)原理簡介(P12)
- 13.2.10 偏心因子與其對應(yīng)狀態(tài)原理(P13)
- 14.2.11 普遍化狀態(tài)方程(P14)
- 15.2.12 混合規(guī)則及虛擬臨界參數(shù)(P15)
- 16.2.13 維里方程混合規(guī)則(P16)
- 17.2.14 立方型狀態(tài)方程混合規(guī)則(P17)
- 18.2.15 液體pvt關(guān)系(P18)
- 19.2.16 流體pvt關(guān)系總結(jié)(P19)
- 20.3.1 熱力學(xué)基本方程(P20)
- 21.3.2 Maxwell關(guān)系式(P21)
- 22.3.3 熱容(P22)
- 23.3.4 理想氣體焓變的計算(P23)
- 24.3.5 理想氣體熵變的計算(P24)
- 25.3.6 剩余性質(zhì)(P25)
- 26.3.7 剩余焓的計算(P26)
- 27.3.8 剩余熵的計算(P27)
- 28.3.9 蒸發(fā)焓和蒸發(fā)熵(P28)
- 29.3.10 過程焓變和熵變計算舉例(P29)
- 30.3.11 熱力學(xué)性質(zhì)圖(P30)
- 31.3.12 水蒸氣表(P31)
- 32.4.1 熱力學(xué)第一定律(P32)
- 33.4.2 熱力學(xué)第二定律(P33)
- 34.4.3 能量的質(zhì)量和級別,4.4理想功、損失功與熱力學(xué)效率,4.4理想功、(P34)
- 35.4.8 氣體的壓縮(P35)
- 36.4.9 氣體的膨脹(P36)
- 37.4.11 制冷循環(huán)(P37)
- 38.4.12 熱泵及其應(yīng)用,4.14 制冷劑和載冷劑的選擇(P38)
- 39.5.1 理想混合物與非理想混合物(P39)
- 40.5.2 非理想混合物系的熱力學(xué)性質(zhì)(P40)
- 41.5.3 偏摩爾熱力學(xué)性質(zhì)的關(guān)系(P41)
- 42.5.4 偏摩爾性質(zhì)的計算(P42)
- 43.5.5 變組成混合物的熱力學(xué)性質(zhì)(P43)
- 44.5.6 純流體的逸度和逸度系數(shù)(P44)
- 45.5.7 混合物的逸度和逸度系數(shù)(P45)
- 46.5.8 活度和活度系數(shù)(P46)
- 47.5.9 活度系數(shù)模型(P47)
- 48.5.10 局部組成型活度系數(shù)方程(P48)
- 49.5.11 活度系數(shù)方程參數(shù)的獲取及活度系數(shù)與溶液的非理想行為(P49)
- 50.6.1 相平衡基礎(chǔ)(P50)
- 51.6.2 互溶系統(tǒng)的VLE關(guān)系式(P51)
- 52.6.3 (γ-Φ)法VLE關(guān)系式化簡(P52)
- 53.6.4 中低壓下的泡露點計算(泡點壓力計算)(P53)
- 54.6.5 中低壓下的泡露點計算(泡點溫度計算)(P54)
- 55.6.6 低壓下汽液平衡計算及舉例(P55)
- 56.6.7 烴類系統(tǒng)K值法(P56)
- 57.6.8 烴類系統(tǒng)K值法計算舉例(P57)
- 58.6.9 閃蒸計算及舉例(P58)
- 59.6.10 高壓汽液平衡(HP-VLE)(P59)
- 60.6.11 二元及三元液液平衡相圖(P60)
- 61.6.12 液液平衡計算(P61)
化工熱力學(xué)的主要任務(wù)是以熱力學(xué)第一、第二定律為基礎(chǔ),研究化工過程中各種能量的相互轉(zhuǎn)化及其有效利用的規(guī)律,研究物質(zhì)狀態(tài)變化與物質(zhì)性質(zhì)之間的關(guān)系以及物理或化學(xué)變化達到平衡的理論極限、條件和狀態(tài)。
第1章緒論
1.掌握化工熱力學(xué)的研究內(nèi)容;
2.掌握化工熱力學(xué)研究特點。
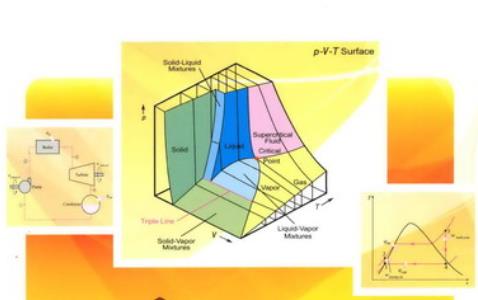
第2章流體的p-V-T(x)關(guān)系
第3章焓、熵、熱容與溫度、壓力的關(guān)系
1.掌握Maxwe11關(guān)系式;
2.掌握剩余性質(zhì);
3.利用二階舍項virial方程計算剩余燴和剩余熵
4.利用立方型狀態(tài)方程計算剩余焙和剩余熵5.利用普遍化第二virial系數(shù)計算剩余焙和剩余熵
6.利用普遍化三參數(shù)壓縮因子法計算剩余燴和剩余熵
7.了解熱力學(xué)性質(zhì)圖表
第4章偏摩爾性質(zhì)、逸度和活度
1.掌握偏摩爾性質(zhì)的定義及計算
2.掌握Gibbs-Duhem方程3.掌握逸度及逸度系數(shù)的定義及計算
4.掌握混合性質(zhì)的定義
由不同物質(zhì)混合形成混合物的過程,特別是形成液體混合物的過程,通常會引起體積效應(yīng)和熱效應(yīng)。這些現(xiàn)象是伴隨著混合過程發(fā)生的。為了表達這種關(guān)系,定義熱力學(xué)函數(shù)混合過程性質(zhì)變化,簡稱混合性質(zhì)。用符號AM表示。
第5章相平衡
1.了解平衡判據(jù)
2.了解汽液平衡相圖
3.掌握活度系數(shù)法計算汽液平衡
4.掌握狀態(tài)方程法計算汽液平衡
5.了解K值法在烴類系統(tǒng)的泡點和露點計算
第6章反應(yīng)熱與反應(yīng)平衡
1.掌握燃燒焙、生成焙與反應(yīng)熱的定義
2.掌握反應(yīng)平衡常數(shù)的定義
第7章化工過程能量分析1.掌握熱力學(xué)第一定律2.掌握理想功、損失功、有效能的定義。
3.掌握化工過程能量分析的三種方法。
第8章壓縮蒸汽動力循環(huán)與制冷
1.掌握氣體的壓縮和膨脹過程的熱力學(xué)分析。